
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
长春高新
000661 |
0.48%
|
最新:68.43
开盘:69.37 昨收:68.1 |
开盘%:1.86%
振幅%:2.42% 换手%:1.34% |
最高:69.77
最低:68.12 量比:0.75 |
总市值:279 亿
流通值:273 亿 成交额:4 亿 |
- 基本信息
- 主力分时图 New
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
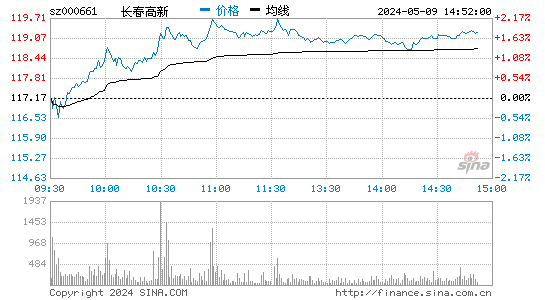
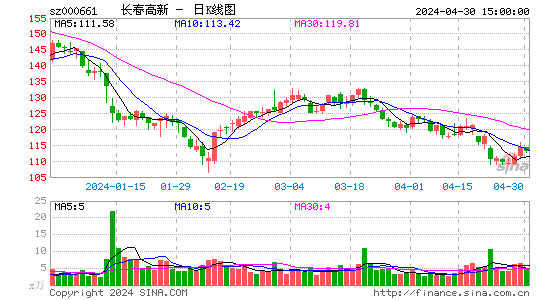
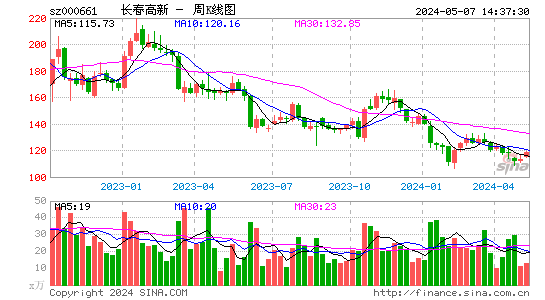
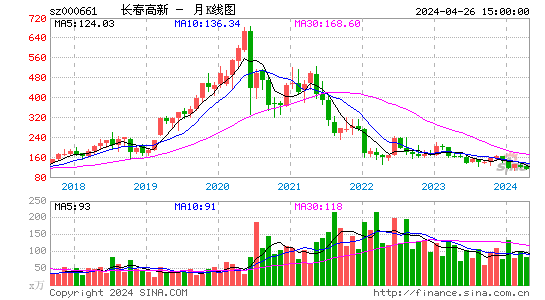
长春高新股票分析
深度解析长春高新股票及其市场表现
公司概况
长春高新是一家集生物制药、疫苗研发、高新技术产业于一体的综合性企业。公司成立于XXXX年,总部位于中国长春市,经过多年的发展,已成为国内生物制药领域的佼佼者。
业务领域
生物制药:长春高新在生物制药领域拥有强大的研发和生产能力,主要产品包括基因工程药物、生物类似药等。
疫苗研发:公司在疫苗研发方面也取得了显著成果,为国内外市场提供了高质量的疫苗产品。
财务表现
从近几年的财务数据来看,长春高新的营业收入和净利润均呈现出稳步增长的趋势。
市场前景
随着国内生物制药市场的不断扩大,长春高新有望凭借其在该领域的领先地位,进一步拓展市场份额。
总结
长春高新作为一家生物制药及高新技术产业公司,拥有强大的研发能力和市场竞争力。在财务表现方面,公司呈现出稳步增长的趋势。未来,随着市场的不断扩大,长春高新有望继续保持强劲的发展势头。
{summary}
长春高新是一家生物制药及高新技术产业公司,涉及生物制药、疫苗研发等多个领域。公司财务表现稳健,市场前景广阔,是投资者关注的热点股票之一。{/summary}
2026-06-03 20:16
【公告精选:兖矿能源拟164.15亿元收购新能源集团及山能售电100%股权;数据港拟不超8亿元采购算力服务】6月3日电,【重要】兖矿能源:拟164.15亿元收购控股股东旗下新能源集团及山能售电100%股权二连板亨通光电:当前全球光纤光缆行业市场环境正常 部分产品单价波动对公司未来业绩影响需综合判断二连板实益达:股权穿透后,公司持有宇树科技约0.01%股权长盈通:下属子公司生一升存在业绩承诺无法实现的风险银之杰:公司“被立案调查”相关传闻不属实【再融资】罗曼股份:拟定增募资不超2.93亿元 用于智能算力集群建设及运营项目曲美家居:境外子公司拟发行不超9亿挪威克朗境外债券百通能源:向特定对象发行股票申请获深交所审核通过【股权变动】必易微:股东拟询价转让3.14%公司股份赛微微电:控股股东拟协议转让不超5.11%公司股份【增减持、回购】生物股份:董事长提议以2亿元—4亿元回购公司股份苑东生物:拟5000万元—1亿元回购股份通策医疗:拟5000万元—1亿元回购股份劲仔食品:拟5000万元—1亿元回购股份久立特材:董秘寿昊添增持1万股公司股份*ST亚士:控股股东拟被动减持3%公司股份鼎胜新材:股东拟合计减持不超3%公司股份方大炭素:拟减持不超8051.94万股已回购股份精研科技:控股股东及其一致行动人、董事拟减持公司不超1.27%股份必易微:股东拟减持不超1.15%公司股份兴业股份:股东拟减持不超1%公司股份奥普光电:控股股东拟减持公司不超1%股份天源迪科:董事长拟减持公司不超0.6272%股份【经营数据】广汽集团:5月新能源汽车销量同比增长71.64%金龙汽车:5月客车销售量同比下降1.85%江铃汽车:5月汽车销量32278辆 同比增长5.98%上港集团:5月预计完成母港集装箱吞吐量479.1万标准箱,同比增长3%【中标合同】金智科技:近期累计中标1.81亿元国家电网下属子公司配网相关项目平治信息:预中标中国移动1.37亿元智算集群项目正和生态:中标1497.79万元工程项目【重大投资】思源电气:控股子公司拟6亿元投资如高高压产能扩充建设项目晶合集成:拟与其他投资方向安徽瑞晶进行增资友发集团:全资子公司与专业投资机构共同投资设立合伙企业【其他】数据港:拟不超8亿元采购算力服务三元生物:年产2万吨阿洛酮糖项目投产鹏鼎控股:收到全资子公司利润分配款10亿元和而泰:拟5250万元受让合伙企业份额电科数字:子公司收到政府补助合计2260万元贵阳银行:董事长张正海因到龄退休辞任京沪高铁:董事长刘洪润因工作调动离任建业股份:2023—2025年度税款及滞纳金已缴纳完毕惠泰医疗:控股子公司取得两项医疗器械注册证长春高新:子公司GenSci155注射液境内生产药品注册临床试验申请获批准云南白药:INB301注射液新药临床试验申请获美国FDA许可ST人福:注射用盐酸兰地洛尔药品注册上市申请获受理福安药业:子公司二氮嗪原料药获得FDA注册批准通知书九强生物:甲状腺素结合力测定试剂盒取得医疗器械注册证
2026-06-03 17:53
长春高新:子公司GenSci155注射液境内生产药品注册临床试验申请获得批准。
2026-06-01 20:21
【公告精选:晋控电力等电力股提示风险;信立泰拟3亿元—5亿元回购股份】6月1日电,【热点】两连板晋控电力:公司现未开展与算力相关的业务两连板江苏国信:目前未开展算电协同业务,也未参与蒙电入苏项目两连板深南电A:公司不涉及算力业务*ST联翔:光芯片资产注入、控制权变更等传闻均为不实信息【并购重组】友发集团:拟6.72亿元收购沧州隆泰迪53%股权声迅股份:拟2.51亿元收购中科锐择51%股权 切入特种光电赛道【再融资】智微智能:拟定增募资不超28.7亿元 用于智算中心建设及运营项目等英派斯:拟定增募资不超3亿元深南电路:筹划向特定对象发行股票西部超导:控股子公司聚能磁体拟申请向不特定合格投资者公开发行股票并在北交所上市海亮股份:发行H股备案申请材料获中国证监会接收【增减持、回购】信立泰:拟3亿元—5亿元回购股份海利得:拟1.5亿元—3亿元回购股份创新医疗:拟5000万元—1亿元回购股份方大集团:拟4000万元—6000万元回购股份华测导航:董事、总经理朴东国拟2500万元—3500万元增持公司股份咸亨国际:股东拟合计减持不超3.62%公司股份云中马:股东拟合计减持不超2.93%公司股份保立佳:董事杨美芹拟减持公司不超2.71%股份矩子科技:股东拟减持公司不超1.41%股份【经营数据】美团:一季度营收910.39亿元 同比增长5.6%比亚迪:5月销量38.35万辆长城汽车:5月份销量10.04万辆,同比下降1.79%上汽集团:5月新能源汽车销量18.25万辆,同比增长46.49%北汽蓝谷:5月销量21871辆,同比增长27.75%赛力斯:5月份销量36480辆,同比下降17.38%汉马科技:5月份新能源中重卡销量1095辆,同比增长21.4%威胜信息:5月合计中标3个项目 中标金额合计约6237.83万元【中标合同】远东股份:5月份子公司中标/签约千万元以上合同订单合计17.97亿元亚通精工:全资子公司亚通重装中标8.6亿元项目宏润建设:中标深蓝航天液体火箭试验基地工程建设项目金冠股份:近期中标合计2.73亿元项目三星电气:签订约1.58亿元马来西亚TNB电力局智能电表项目金诚信:续签约1.25亿元老挝开元钾盐矿委托采矿运营管理承包合同三星电气:子公司预中标约1.14亿元国家电网采购项目鸿富瀚:控股子公司中标整机柜液冷部件—冷板产品【重大投资】英派斯:拟约6.59亿元投建海南智慧体育产业园项目华兰股份:子公司拟向自然常数增资2.05亿元万润新能:拟对参股公司磷化万润增资8820万元浙江黎明:与专业投资机构共同投资厦门星文耀安创业投资合伙企业(有限合伙)华斯股份:拟在新疆喀什投资设立全资子公司天龙股份:拟出资3180万元与私募基金合作投资东鹏控股:全资子公司拟出资2006万元获取德盈星途14.93%股权鼎龙科技:拟投资1000万元认购守正基金部分股权【其他】牧原股份:选举曹治年为董事长华泰股份:年产15万吨高得率本色木纤维配套年产4.5万吨木质素项目进入调试运行阶段广安爱众:控股孙公司奇台恒众风电项目进入商业运行海思科:与礼来公司签署授权与研发合作协议亚威股份:拟与Haco开展股权和技术合作中科三环:赵寅鹏不再代行公司总裁职权,将继续在公司担任董事长职务淮北矿业:董事、总经理邱丹因工作调动辞职铂科新材:筹划发行H股股票并在香港联交所主板上市九洲集团:部分新能源电站收到可再生能源发电补贴合计1.33亿元芯源微:控股子公司收到3522万元政府补助永茂泰:子公司收到1061.59万元政府补助宏源药业:补缴2025年度企业所得税税款1856.73万元深振业A:拟1.5亿元出售5项深圳地区自有物业尚纬股份:拟将证券简称变更为“福华尚纬”百傲化学:股东终止协议转让公司股份和仁科技:终止筹划控制权变更事项 2日复牌新金路:实控人、董事长刘江东减持计划提前终止银河电子:控股股东未减持公司股份并提前终止减持计划卡倍亿:终止向不特定对象发行可转债并撤回申请文件盛帮股份:终止收购无锡沃可发动机降噪部件有限公司60%股权千禾味业发布未来三年股东回报规划 每年度现金分红总额占净利润比例不低于90%*ST中地:6月3日起撤销退市风险警示健康元:重组人促卵泡激素注射液获得药品注册证书健康元:莱康奇塔单抗注射液上市许可申请获受理丽珠集团:获得重组人促卵泡激素注射液药品注册证书翰宇药业:卡贝缩宫素原料药获得欧盟DCP核准新华制药:获得碳酸司维拉姆干混悬剂药品注册证书华纳药厂:法罗培南钠片获药品注册证书长春高新:注射用GenSci136、GenSci145片临床试验申请获FDA批准卫光生物:人凝血因子Ⅸ药物临床试验获批准昂利康:子公司获得异氟烷药品注册证书达嘉维康:子公司获得阿奇霉素干混悬剂药品注册证书西点药业:子公司获得维生素B12注射液药品注册证书福元医药:甲巯咪唑片获药品注册证书同和药业:塞来昔布原料药通过CDE审批
2026-06-01 16:55
【长春高新:子公司注射用GenSci136获FDA批准开展临床试验】6月1日电,长春高新(000661.SZ)公告称,公司子公司金赛药业收到美国FDA批准文件,同意注射用GenSci136在美国开展临床试验,适应症为重症肌无力。该药品为自主研发的BCMA三聚体融合蛋白,属治疗用生物制品1类药物,有望为患者提供更优治疗选择。
2026-06-01 16:55
【长春高新:子公司GenSci145片获FDA批准开展临床试验】6月1日电,长春高新(000661.SZ)公告称,公司子公司金赛药业收到美国FDA批准文件,同意GenSci145片在美国开展临床试验,适应症为携带PIK3CA突变的局部晚期或转移性实体瘤。该药为新型突变选择性PI3Kα抑制剂,临床前研究显示对多种PIK3CA热点突变有选择性抑制活性,且具血脑屏障穿透能力。此前,该药境内临床试验申请已获国家药监局批准。
2026-06-01 16:53
长春高新:子公司注射用GenSci136境外生产药品注册临床试验申请获得批准。
2026-05-29 16:55
长春高新:甲磺酸亮丙瑞林注射液(6M)上市申请获得受理。
2026-05-26 16:02
【长春高新:子公司GenSci144片临床试验申请获批准】5月26日电,长春高新(000661.SZ)公告称,公司子公司金赛药业收到国家药监局核准签发的《药物临床试验批准通知书》,GenSci144片境内生产药品注册临床试验申请获得批准,拟用于苯丙酮尿症(PKU)的治疗。该药品为口服小分子抑制剂,可降低血苯丙氨酸水平,为PKU患者提供新治疗选择。
2026-05-25 16:07
长春高新:子公司GenSci144片境内生产药品注册临床试验申请获得受理。
2026-05-15 20:00
长春高新:子公司GenSci161注射液境外生产药品临床试验申请获得批准。
2026-05-15 20:00
【长春高新:子公司GenSci161注射液获美国FDA批准开展临床试验】5月15日电,长春高新(000661.SZ)公告称,公司子公司金赛药业收到美国FDA批准文件,同意GenSci161注射液在美国开展临床试验,用于治疗化脓性汗腺炎。该药品为全人源化双特异性抗体,可同时靶向IL-1α和IL-1β,有望改善中重度患者治疗效果。此前,该药在国内已获批用于子宫内膜异位症等适应症的临床试验。
2026-05-12 20:12
【长春高新:子公司伏欣奇拜单抗注射液获得药物临床试验批准通知书】长春高新5月12日公告,公司子公司长春金赛药业有限责任公司收到国家药品监督管理局核准签发的伏欣奇拜单抗注射液《药物临床试验批准通知书》。伏欣奇拜单抗是金赛药业研发的一款全人源抗白介素-1β(IL-1β)单抗,拟用于治疗在启动降尿酸治疗初期的痛风患者中降低急性发作风险适应症。在启动降尿酸治疗初期的痛风患者中降低急性发作风险。由于医药产品具有高科技、高风险、高附加值的特点,药品的前期研发以及产品从研制、临床试验报批到投产的周期长、环节多,容易受到一些不确定性因素的影响,本次临床试验进程尚存在不确定性。
2026-05-12 19:56
【长春高新:子公司伏欣奇拜单抗注射液临床试验申请获批准】5月12日电,长春高新(000661.SZ)公告称,子公司金赛药业伏欣奇拜单抗注射液境内生产药品注册临床试验申请获得国家药监局批准,同意开展用于降低启动降尿酸治疗初期痛风患者急性发作风险的临床试验。
2026-05-06 20:32
【长春高新:子公司GenSci155注射液临床试验申请获受理】5月6日电,长春高新(000661.SZ)公告称,公司控股子公司金赛药业自主研发的GenSci155注射液境内生产药品注册临床试验申请已获国家药监局受理。该药品为长效化脂肪酸偶联重组人胰岛素样生长因子-1类似物,拟用于预防早产儿支气管肺发育不良和急性缺血性卒中。
2026-05-06 19:30
长春高新:子公司GenSci155注射液境内生产药品注册临床试验申请获得受理。
2026-05-06 19:29
长春高新:子公司伏欣奇拜单抗注射液在境内获批上市。
2026-04-28 17:02
长春高新:子公司GenSci161注射液境内生产药品注册临床试验申请获得批准,子公司GenSci164注射液境内生产药品注册临床试验申请获得受理。
2026-04-22 22:03
【公告精选:拓斯达一季度净利同比增1147.36%;中国船舶下属子公司签订约90亿元重大造船合同】4月22日电,【经营数据】拓斯达:一季度净利润4808.33万元 同比增长1147.36%大宏立:一季度净利润1061.73万元 同比增长937.58%恩捷股份:一季度净利润2.6亿元 同比增长901.7%永创智能:2025年净利润同比增长780.87% 拟10派0.8元盛达资源:一季度净利同比预增744.99%—986.42%移为通信:一季度净利润5192.99万元 同比增长430.64%东岳硅材:有机硅产品毛利率显著提升 一季度净利润同比增长426.99%友好集团:2025年净利润同比增长316.27%康辰药业:2025年净利润同比增长293.13% 拟10派3.5元乐普医疗:2025年净利润同比增长289.57% 拟10派1.6275元旗天科技:一季度净利润同比增长264.52%银河微电:车规级产品产销规模扩大 一季度净利润同比增长200.15%中光防雷:一季度净利润818.37万元 同比增长191.18%高铁电气:一季度净利润同比增长150.92%贝达药业:一季度净利润2.36亿元 同比增长135.71%华光新材:2025年净利润同比增长133.29% 拟10派4.7元西藏珠峰:2025年净利润同比增长123% 拟10派0.2元智明达:一季度净利润同比增长114.44%同花顺:一季度净利润2.56亿元 同比增长112.58%东材科技:一季度净利润1.87亿元 同比增长103.35%联泓新科:一季度净利润1.45亿元 同比增长102.67%震裕科技:2025年净利润同比增长101.98% 拟10转4派3元巨化股份:2025年净利润同比增长94.29% 拟10派3.8元青达环保:2025年净利润同比增长88.16% 拟10转4派2.8元敷尔佳:一季度净利润1.72亿元 同比增长87.73%甘李药业:2025年净利润同比增长86.05% 拟10派10元昂立教育:经营效率提升 一季度净利润同比增长84.71%厦钨新能:公司产品量价齐升 一季度净利润同比增长79.17%永创智能:一季度净利润7129.56万元 同比增长75.26%圣农发展:一季度净利润2.53亿元 同比增长71.41%北特科技:2025年净利润同比增长67.35% 拟10派1.39元德赛电池:一季度净利润7991.65万元 同比增长64.23%圆通速递:一季度净利润同比增长60.76%光迅科技:一季度净利润2.4亿元 同比增长59.76%东材科技:2025年净利润同比增长57.68% 拟10派0.5元艾力斯:一季度净利润同比增长54.94%莲花控股:2025年净利润同比增长52.59% 规模和效益再创新高视源股份:一季度净利润2.47亿元 同比增长52.45%健盛集团:一季度净利润同比增长51.92%寒锐钴业:铜产品销售量价齐升 一季度净利润同比增长51.07%德力佳:一季度净利润同比增长48.91%山河药辅:2025年净利润同比增长47.84% 拟10派3元璞泰来:一季度净利润7.04亿元 同比增长44.37%光迅科技:2025年净利润9.46亿元 同比增长43.1%西藏珠峰:一季度净利润1.8亿元 同比增长42.73%莲花控股:一季度净利润同比增长42.06%锡华科技:2025年净利润同比增长41.85% 拟每股派0.16元厦钨新能:2025年净利润同比增长41.82% 拟10派3元瑞纳智能:2025年净利润1.09亿元,同比增长41.72%国脉文化:2025年净利润同比增长41.63% 拟10派0.18元三峡水利:2025年净利润同比增长40.75% 拟10派0.75元久吾高科:2025年净利润同比增长38.97% 拟10派2.5元国脉文化:一季度净利润同比增长35.56%盛达资源:2025年净利润5.25亿元 同比增长34.73%节能国祯:一季度净利润9004.89万元 同比增长32.69%蓝色光标:一季度净利润1.26亿元 同比增长32.04%罗莱生活:一季度净利润1.48亿元 同比增长30.54%雷赛智能:一季度净利润7212.03万元 同比增长29.2%军信股份:一季度净利润2.2亿元 同比增长27.09%华电能源:一季度净利润同比增长26.15%四方达:一季度净利润4292.89万元 同比增长25.66%小商品城:一季度净利润9.9亿元 同比增长23.29%钢研高纳:一季度净利润6739.48万元 同比增长22.42%恒瑞医药:一季度净利润同比增长21.78% 力争全年创新药销售收入实现超过30%的增长华电能源:2025年净利润同比增长20.81%罗莱生活:2025年净利润同比增长20.1% 拟10派4.2元金力永磁:2026年一季度净利润1.93亿元 同比增长20.09%润本股份:一季度净利润同比增长19.09%龙头股份:2025年净利润同比增长17.66% 拟10派0.388元天银机电:一季度净利润1028.72万元 同比增长17.42%熵基科技:2025年净利润同比增长17.3% 拟10派4.8元城发环境:一季度净利润3.14亿元 同比增长15.1%齐鲁银行:一季度归母净利润同比增长14.01%雷赛智能:2025年净利润同比增长12.42% 拟10派2.5元科博达:2025年净利润同比增长12.34% 拟10派6.2元水晶光电:一季度净利润2.47亿元 同比增长11.69%铂科新材:2025年净利润同比增长11.29% 拟10转4派2元银河微电:2025年净利润同比增长11.17% 拟10派2.5元广立微:2025年净利润同比增长10.49% 拟10派2元华翔股份:一季度净利润同比增长10.41%中信特钢:一季度净利润15.11亿元 同比增长9.23%中谷物流:2025年净利润同比增长9.03% 拟10派2.4元盐田港:一季度净利润3.41亿元 同比增长8.85%老白干酒:一季度净利润1.65亿元 同比增长8.55%古越龙山:2025年净利润同比增长8.14% 拟10派0.9元圆通速递:2025年净利润同比增长7.73% 拟10派2.5元埃泰克:一季度净利润同比增长7.32%盐田港:2025年净利润同比增长7.28% 拟10派1.07元尤洛卡:一季度净利润1416.45万元 同比增长6.83%乾照光电:一季度净利润2964.06万元 同比增长6.59%劲仔食品:一季度净利润7124.67万元 同比增长5.48%杰克科技:2025年净利润同比增长5.38% 拟10派4.5元古越龙山:一季度净利润同比增长5.1%成都银行:一季度净利润同比增长4.81%润本股份:2025年净利润同比增长4.78% 拟10派2.6元瑞迪智驱:2025年净利润同比增长4.01% 拟10转4派2元成都银行:2025年净利润同比增长3.31% 拟10派9.21元南钢股份:一季度净利润同比增长3.23%精华制药:2025年净利润同比增长3.12% 拟10派0.9元万马股份:2025年净利润同比增长1.74% 拟10派0.55元贵阳银行:2025年净利润同比增长1.66% 拟10派3元沪农商行:一季度净利润同比增长0.73%翔楼新材:2025年净利润同比增长0.62% 拟10转4.5派7元沪农商行:2025年净利润123.13亿元,同比增长0.20%恩捷股份:2025年净利润1.43亿元 同比扭亏昂立教育:2025年净利润8657.02万元 同比扭亏冠城新材:2025年净利润7468.16万元同比扭亏 拟10派0.3元三峡水利:一季度净利润3232.46万元 同比扭亏为盈宜宾纸业:2025年净利润2734.02万元 同比扭亏为盈南京化纤:一季度净利润1215.05万元 同比扭亏为盈赛摩智能:一季度净利润520.05万元 同比扭亏为盈北鼎股份:一季度净利润3276.06万元 同比下降1.83%电科蓝天:2025年净利润同比下降3.02% 拟10派0.7463元安科瑞:一季度净利润5027.32万元 同比下降3.65%百合花:2025年净利润同比下降5.18% 拟10派1.3元欧普康视:一季度净利润1.46亿元 同比下降8.79%久吾高科:一季度净利润1582.89万元 同比下降10.39%毓恬冠佳:一季度净利润同比下降10.85%哈铁科技:2025年净利润同比下降11.55% 拟10派1.2元华策影视:一季度净利润8125.94万元 同比下降11.78%旭升集团:2025年净利润同比下降12.28% 拟每股派0.16元瑞迪智驱:一季度净利润2027.41万元 同比下降13.86%盈康生命:一季度净利润2575.8万元 同比下降14.12%豪恩汽电:一季度净利润同比下降15.15%锡华科技:一季度净利润同比下降16.26%劲仔食品:2025年净利润同比下降16.68% 拟10派3元铁科轨道:一季度净利润同比下降17.7%华能蒙电:2025年净利润同比下降17.97% 拟10派2.2元利安科技:2025年净利润同比下降18.42% 拟10派2元华策影视:2025年净利润同比下降21.36% 拟10派0.11元隧道股份:2025年净利润同比下降22.07% 拟10派1.2元科博达:一季度净利润同比下降22.41%银星能源:一季度净利润5547.81万元 同比下降23.55%贝达药业:2025年净利润同比下降24.15% 拟10派1.5元贵州燃气:2025年净利润同比下降24.62% 拟10派0.1446元龙高股份:一季度净利润同比下降25.99%金卡智能:2025年净利润同比下降26.16% 拟10派2.5元重庆路桥:2025年净利润同比下降27.59% 拟10派0.26元通光线缆:一季度净利润401.28万元 同比下降28.15%长盈精密:一季度净利润1.25亿元 同比下降28.39%新天科技:一季度净利润1943.15万元 同比下降28.58%德赛电池:2025年净利润同比下降29.23% 拟10派2.3元金卡智能:一季度净利润2971.79万元 同比下降32%苏盐井神:2025年净利润同比下降32.11% 拟10派2.52元苏盐井神:一季度净利润同比下降32.33%爱美客:一季度净利润2.98亿元 同比下降32.79%敷尔佳:2025年净利润同比下降34.56% 拟10派8元奥特维:一季度净利润同比下降35.42%武进不锈:2025年净利润同比下降36.67% 拟10派0.5元乖宝宠物:一季度净利润1.24亿元 同比下降39.5%大禹节水:2025年净利润同比下降39.72% 拟10派0.2元泰晶科技:2025年净利润同比下降40.37% 拟10派0.41元老白干酒:2025年净利润同比下降45.4% 拟10派2元国城矿业:一季度净利润3.53亿元 同比下降52.47%飞龙股份:一季度净利润5783.5万元 同比下降52.84%万孚生物:一季度净利润8439.95万元 同比下降55.38%戴维医疗:一季度净利润同比下降56.19%天舟文化:一季度净利润1006.73万元 同比下降58.5%川宁生物:一季度净利润1.11亿元 同比下降61.58%工大高科:2025年净利润同比下降61.65% 拟10派1.1元云南锗业:2025年净利润同比下降62.06% 拟10派0.1元奥特维:2025年净利润同比下降64.64% 拟10派8元开尔新材:一季度净利润388.66万元 同比下降70.16%红宝丽:2025年净利润同比下降70.36% 拟10派0.3元合众思壮:一季度净利润同比下降84.25%工大高科:一季度净利润同比下降86.59%宏昌科技:一季度净利润同比下降87.96%神州细胞:2025年亏损5.65亿元 同比由盈转亏七一二:2025年亏损4.92亿元东风股份:2025年亏损4.8亿元 同比由盈转亏东软集团:2025年亏损3.58亿元 同比由盈转亏火星人:2025年亏损2.96亿元国新能源:2025年亏损2.85亿元永臻股份:2025年亏损2.21亿元 同比转亏拓日新能:2025年亏损1.99亿元 同比由盈转亏东芯股份:2025年亏损1.95亿元正和生态:2025年亏损1.57亿元盛科通信:2025年亏损1.5亿元福建水泥:2025年亏损1.27亿元南京化纤:2025年亏损9994.22万元 同比亏损收窄坤彩科技:2025年亏损9205.37万元 拟10送3派1.5元东亚药业:2025年亏损8239.2万元拓尔思:一季度亏损7740.69万元帝奥微:2025年亏损6597.74万元 拟10派1元品高股份:2025年亏损5251.55万元赛微电子:一季度亏损4909.90万元 由盈转亏裕兴股份:一季度亏损4861.02万元中望软件:一季度亏损3830.45万元恒尚节能:2025年亏损3502.43万元友讯达:一季度亏损3223.2万元 同比由盈转亏飞天诚信:一季度亏损2789.72万元帝奥微:一季度亏损2465.23万元 同比由盈转亏红宝丽:一季度亏损2401.2万元武进不锈:一季度亏损1755.37万元 同比转亏*ST凯鑫:一季度亏损1126.76万元 同比转亏海顺新材:一季度亏损1083.09万元博汇科技:一季度亏损786.98万元创益通:2025年亏损319.46万元 同比由盈转亏中英科技:一季度亏损110.54万元中国化学:1月—3月合同总额1149.14亿元中油工程:一季度累计实现新签合同额同比增长7.28%西昌电力:一季度水力发电站发电量同比增长9.13%凤凰股份:1—3月商品房合同销售金额同比减少28.31%【增减持、回购】乖宝宠物:拟1亿元—2亿元回购股份科思股份:拟3000万元—6000万元回购股份顺钠股份:股东邵伟华拟减持公司不超3%股份【中标合同】中国船舶:下属子公司签订约90亿元重大造船合同华康洁净:联合中标1.06亿元工程总承包项目金螳螂:越南孙公司签署约4亿元工程项目【重大投资】德赛电池:子公司拟投资不超25亿元开展消费电芯业务科达利:拟不超12亿元投建锂电池精密结构件四期项目顾家家居:拟不超11.88亿元投建产业总部项目四方达:控股子公司拟约4.5亿元投建CVD金刚石项目【其他】法尔胜:公司业务不涉及“光纤”“特种光纤”,不存在“重组”“被借壳”的情形柳钢股份:筹划收购广西钢铁部分少数股权 股票4月23日停牌艾比森:拟发行可转债募资不超8.2亿元南京化纤:公司股票4月23日停牌一天 4月24日起实施退市风险警示新天药业:收到全资子公司分红款2200万元万华化学:蓬莱工业园PDH、POCHP装置将于4月26日停产检修 预计检修30天左右欢瑞世纪:因涉嫌信披违法违规被中国证监会立案傲农生物:因涉嫌信披违法违规被证监会立案兰石重装:公司及控股股东涉嫌信息披露违法违规被中国证监会立案京北方:控股股东终止协议转让公司3702.31万股股份长春高新:子公司GenSci144片境内生产药品注册临床试验申请获受理立方制药:盐酸伊伐布雷定和美阿沙坦钾原料药上市申请获批准华东医药:子公司独家商业化产品CXG87上市许可申请获受理赛升药业:子公司收到达格列净化学原料药上市申请批准通知书
2026-04-22 18:41
【长春高新:子公司GenSci144片临床试验申请获受理】4月22日电,长春高新(000661.SZ)公告称,公司控股子公司长春金赛药业有限责任公司近日收到国家药品监督管理局核准签发的《受理通知书》,其自主研发的GenSci144片境内生产药品注册临床试验申请获得受理。GenSci144片是一款口服小分子SLC6A19抑制剂,注册分类为化药1类,拟用于苯丙酮尿症(PKU)的治疗。该药物通过抑制SLC6A19介导的肾小管对苯丙氨酸的重吸收,降低血苯丙氨酸水平,适用于不同类型的PKU患者。此次申请获受理有利于公司拓宽业务结构、优化产品结构,丰富战略领域产品线布局。鉴于医药研发具有高风险、长周期等特点,后续进展存在不确定性,敬请投资者注意投资风险。
2026-04-22 18:36
长春高新:子公司GenSci144片境内生产药品注册临床试验申请获得受理。
2026-04-21 21:52
【公告精选:华绿生物一季度净利增长超70倍;光线传媒拟出售所持当虹科技不超4%股份】4月21日电,【经营数据】华绿生物:一季度净利润1.1亿元 同比增长7014.32%广东明珠:2025年净利润同比增长3243.47% 拟10派2.13元光线传媒:2025年净利润同比增长472.62% 拟10派1.5元恒誉环保:一季度净利润同比增长414.07%科兴制药:2025年净利润同比增长394.17% 拟10派2.5元南都物业:2025年净利润同比增长353.09% 拟每股派现0.2141元杭电股份:子公司永特信息光纤量价齐升 一季度净利润同比增长279.96%巨一科技:2025年净利润同比增长279.77% 拟10派2元中孚实业:一季度净利润同比增长256.61%众兴菌业:一季度净利润1.63亿元 同比增长237.55%奥来德:蒸发源设备业务收入大幅增长 一季度净利润同比增长214.86%金丹科技:2025年净利润同比增长205.92% 拟10派1元新安股份:2025年净利润同比增长185.67% 拟10派1元光庭信息:2025年净利润同比增长150.85% 拟10转4派3元中孚实业:2025年净利润同比增长129.83% 拟10派1.75元全志科技:一季度净利润2.03亿元 同比增长121.77%回天新材:2025年净利润同比增长116.58% 拟10派1.5元蠡湖股份:一季度净利润同比增长113.69%远东股份:智能电池储能/算力AI板块收入增加 一季度净利润同比增长110.36%天舟文化:2025年净利润同比增长106.43%兴齐眼药:2025年净利润同比增长105.84% 拟10转4.5派10元紫金矿业:一季度净利润同比增长97.5%恒力石化:一季度净利润同比增长90.65%恒达新材:一季度净利润2502.74万元 同比增长89.14%广大特材:2025年净利润同比增长79.6%新黄浦:一季度净利润同比增长78.26%华锐精密:2025年净利润同比增长74.5% 拟10转4派6元华正新材:一季度净利润同比增长68.04%顺网科技:2025年净利润同比增长65.8% 拟10派1.2元融捷健康:2025年净利润同比增长59.65%瑞芯微:一季度净利润3.29亿元 同比增长57.15%威奥股份:2025年净利润同比增长55.2% 拟10派1元兴通股份:一季度净利润1.11亿元 同比增长51.11%格林美:2025年净利润同比增长54.87% 拟10派0.95元银龙股份:2025年净利润同比增长54.51% 拟10派0.7元赛分科技:一季度净利润同比增长49.66%康泰生物:一季度净利润同比增长48.61%赛分科技:2025年净利润同比增长48.59% 拟10派0.7元艾迪精密:一季度净利润同比增长48.39%东宏股份:2025年净利润同比增长47.35% 拟10派2.31元中触媒:2025年净利润同比增长40.76% 拟10转3派2元唯特偶:一季度净利润2975.32万元 同比增长36.72%药石科技:一季度净利润4888.66万元 同比增长36.59%骆驼股份:2025年净利润同比增长36.46% 拟10派3.6元春秋电子:2025年净利润同比增长34.82% 拟10派2元长城科技:2025年净利润同比增长33.62% 拟10派12元佰仁医疗:2025年净利润同比增长32.28% 拟10派8元东方电缆:一季度净利润同比增长32.26%龙净环保:一季度净利润同比增长31.89%惠泉啤酒:一季度净利润同比增长30.2%多浦乐:2025年净利润同比增长28.85% 拟10转4.5派1.08元东山精密:2025年净利润同比增长27.67%佰仁医疗:一季度净利润同比增长27.29%易德龙:2025年净利润同比增长20.66% 拟10派6元王子新材:一季度净利润1008.3万元 同比增长19.8%苑东生物:2025年净利润同比增长19.24% 拟10派4.9元新澳股份:一季度净利润同比增长18.62%恒达新材:2025年净利润同比增长17.32% 拟10派4元海欣股份:2025年净利润同比增长16.6% 拟10派0.5元联瑞新材:2025年净利润同比增长16.42% 拟10派5元大连重工:一季度净利润2.08亿元 同比增长16.17%映翰通:2025年净利润同比增长14.73% 拟10派1.1元英联股份:一季度净利润1252.42万元 同比增长13.41%皇马科技:一季度净利润同比增长10.47%众望布艺:2025年净利润同比下降9.79% 拟10派5元皇马科技:2025年净利润同比增长9.76% 拟10派2.25元飞凯材料:一季度净利润同比增长9.57%泛亚微透:2025年净利润同比增长9.49% 拟10派3.5元天富能源:2025年净利润同比增长7.26% 拟10派0.84元芯瑞达:2025年净利润同比增长5.90% 拟10派2.5元特力A:2025年净利润同比增长4.56% 拟10派1.1元恒勃股份:2025年净利润同比增长4.07% 拟10转4派3元富奥股份:2025年净利润同比增长3.91% 拟10派1.5元山东墨龙:一季度净利润558.4万元 同比增长2.96%稳健医疗:一季度净利润2.51亿元 同比增长1.18%华绿生物:2025年净利润1.1亿元同比扭亏 拟10转3派5元大恒科技:2025年净利润1.04亿元同比扭亏 拟10派0.24元远东股份:2025年营收创新高、净利同比扭亏 拟10派0.1元百利电气:2025年净利润8905.65万元同比扭亏 拟10派0.25元凯美特气:2025年净利润6855.57万元同比扭亏 拟10派0.5元英联股份:2025年净利润3529.25万元同比扭亏 拟10派0.25元博众精工:一季度净利润2847.9万元 同比扭亏为盈智光电气:一季度净利润2279.56万元 同比扭亏为盈中威电子:一季度净利润202.8万元 同比扭亏为盈集智股份:2025年净利润同比下降0.81% 拟10派0.5元天富龙:2025年净利润同比下降2.59% 拟每股派0.25元柏诚股份:2025年净利润同比下降3.34% 拟10派0.7元珀莱雅:2025年净利润同比下降3.5% 拟10派12元光华股份:一季度净利润2458.24万元 同比下降3.75%捷佳伟创业绩快报:2025年净利润26.17亿元 同比下降5.3%珀莱雅:一季度净利润同比下降6.05%万控智造:2025年净利润同比下降7.16% 拟10派0.8元天富龙:一季度净利润同比下降9.02%捷捷微电:一季度净利润1亿元 同比下降10.32%唯特偶:2025年净利润同比下降11.82% 拟10转4.5派5元上海机电:一季度净利润同比下降12.32%宝信软件:一季度净利润同比下降14.25%五芳斋:2025年净利润同比下降14.44% 拟10派5元福耀玻璃:一季度净利润同比下降15.68%苑东生物:一季度净利润同比下降16.11%药石科技:2025年净利润同比下降16.31% 拟10派2.8元新黄浦:2025年净利润同比下降17.25% 拟10派0.31元中国联通:一季度净利润同比下降18% 算力业务收入154亿元陆家嘴:2025年净利润同比下降18.74% 拟10派0.6元长城科技:一季度净利润同比下降18.79%玉马科技:2025年净利润同比下降19.84% 拟10派2元三博脑科:2025年净利润同比下降19.85%万朗磁塑:2025年净利润同比下降19.92% 拟10派1.8元光华股份:2025年净利润同比下降20.88% 拟10派3.6元集智股份:一季度净利润660.38万元 同比下降21.63%中触媒:一季度净利润同比下降22.31%兴通股份:2025年净利润同比下降22.95% 拟10派2元富奥股份:一季度净利润1.25亿元 同比下降23.64%立华股份:一季度净利润1.55亿元 同比下降24.85%苏垦农发:2025年净利润同比下降24.96% 拟10派1.5元威奥股份:一季度净利润同比下降26.07%易德龙:一季度净利润同比下降26.92%大胜达:2025年净利润同比下降27.42% 拟10派0.4244元洪通燃气:2025年净利润同比下降29.77% 拟10派2元正海磁材:一季度净利润4704.91万元 同比下降32.29%芯瑞达:一季度净利润3046.13万元 同比下降33.78%蓝天燃气:一季度净利润同比下降35.01%高盟新材:一季度净利润2463.92万元 同比下降36.2%润和软件:2025年净利润同比下降39.81% 拟10派0.7元众望布艺:一季度净利润同比下降40.43%长春高新:一季度净利润2.76亿元 同比下降41.67%矽电股份:2025年净利润同比下降42.5% 拟10派2.54元温氏股份:2025年净利润同比下降43.25% 拟10派2元蓝天燃气:2025年净利润同比下降43.98%海南机场:2025年净利润同比下降52.33% 拟10派0.05元捷佳伟创:一季度净利同比预降54.81%—65.4%映翰通:一季度净利润同比下降58.28%立华股份:2025年净利润同比下降62.01% 拟10派2.5元凯美特气:一季度净利润1073.2万元 同比下降66.2%陆家嘴:一季度净利润同比下降68.41%广大特材:一季度净利润同比下降92.91%中英科技:2025年净利润同比下降93.28%长春高新:2025年净利润同比下降94% 拟10派1.6元光线传媒:一季度净利润2327.56万元 同比下降98.85%龙利得:一季度亏损338.5万元矽电股份:一季度亏损1039.88万元 同比由盈转亏中巨芯:2025年亏损1659.62万元 同比由盈转亏中国卫星:一季度亏损4269.02万元帅丰电器:2025年亏损5642.12万元 同比由盈转亏云煤能源:一季度亏损9731.81万元良品铺子:2025年亏损1.48亿元 拟10派2.49元王子新材:2025年亏损1.58亿元德尔未来:2025年亏损2.21亿元大龙地产:2025年亏损2.54亿元云煤能源:2025年亏损4.86亿元温氏股份:一季度亏损10.7亿元牧原股份:一季度亏损12.15亿元【热点】3天2板泰晶科技:光模块相关业务尚处于市场推广期 业务收入占比极小合力泰:算力租赁服务已确认的业务收入不足万元3天2板江顺科技:目前未有国内外数据中心液冷板产品销售顺灏股份:公司仅作为投资人参股轨道辰光 其主营业务尚未实现销售收入皮阿诺:控股股东变更为初芯微【再融资】帝科股份:拟定增募资不超30亿元 用于年产2000吨贱金属少银光伏浆料等项目恒勃股份:拟定增募资不超18亿元 用于马来西亚PEEK精密零部件产业化等项目翔丰华:拟定增募资不超6亿元 用于年产9.3万吨新能源电池负极材料项目【增减持、回购】科拓生物:拟1亿元—1.5亿元回购股份光线传媒:拟出售所持当虹科技不超4%股份太阳电缆:象屿集团及其一致行动人拟减持公司不超3%股份唯捷创芯:股东及其一致行动人拟减持不超2%公司股份【中标合同】江河集团:中标2.74亿元利雅得幕墙工程项目华光环能:控股孙公司中标1.35亿元总承包项目腾达建设:中标6523.63万元项目【重大投资】玉马科技:拟4亿元投建年产1600万平方米功能性遮阳新材料建设项目【其他】博济医药:与普什制药签订技术转让合同瀚蓝环境:筹划购买高质量基金100%财产份额及粤丰环保7.22%股份 股票4月22日停牌同德化工:被债权人申请重整及预重整ST中迪:公司股票交易被叠加实施退市风险警示并继续实施其他风险警示万科A:23万科MTN001将于4月23日兑付本息合计8.65亿元润都股份:盐酸去甲乌药碱化学原料药上市申请获批准
2026-04-19 11:29
【长春高新:目前美国关税政策对公司业务无影响】4月19日电,长春高新4月19日在互动平台表示,目前美国关税政策对公司业务无影响。
2026-04-16 17:25
【长春高新:子公司注射用GenSci136临床试验申请获批准】4月16日电,长春高新(000661.SZ)公告称,公司子公司长春金赛药业有限责任公司近日收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,其自主研发的注射用GenSci136境内生产药品注册临床试验申请获得批准。该药品为治疗用生物制品1类药物,适应症为全身型重症肌无力(gMG)。此前,该药品用于治疗眼肌型重症肌无力(oMG)的临床试验申请已获受理,用于治疗免疫球蛋白A肾病(IgAN)的临床试验申请已获批准。由于医药研发具有高风险、长周期等特点,本次临床试验进程尚存在不确定性,敬请投资者注意投资风险。公司将积极推进研发项目并履行信息披露义务。
2026-04-16 17:25
【长春高新:子公司GS3-007a干混悬剂临床试验申请获批准】4月16日电,长春高新(000661.SZ)公告称,公司控股子公司长春金赛药业有限责任公司近日收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,其自主研发的GS3-007a干混悬剂境内生产药品注册临床试验申请获得批准。该药品为口服小分子生长激素促分泌药物,注册分类为化药1类,拟用于特发性身材矮小(ISS)的治疗。截至目前,国内尚无同类产品上市。此次获批符合公司在儿童健康领域的战略规划,将推动后续产品临床开发。鉴于医药研发具有高风险及不确定性,敬请投资者注意投资风险。
2026-04-16 17:24
长春高新:子公司注射用GenSci136境内生产药品注册临床试验申请获得批准。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 股市投资:大跌胆要大,大涨胆要小
- 股市夺命三绝:精准把握买卖点的实战策略
- 炒股致富的曲折历程与人生抉择
- 炒股必修课:深度解析成交量绿柱的奥秘与市场策略
- 半路板交易的深度剖析与策略构建
- 股票投资:深入解析技术面分析要点与实战策略
- 股市高手的智慧结晶:掌握这些铁律,稳健盈利不再是梦
- 情绪周期与股市操作策略:精准把握,稳健前行
- 成交量变化八阶律:洞悉股市风云的钥匙
- 龙头战法的深度剖析与实战智慧
- 股市航行:精准策略降低投资风险
- 中国经济结构调整下的投资新机遇
- 股市智慧:掌握六大心态,解锁盈利之门
- 掌握三大原则,轻松预判金银涨跌
- 牛市操作经验深度剖析
- 散户股市实战策略:精准把脉市场,高效布局赢在智取
- 掌握集合竞价超预期战法,洞悉股市先机
- 股市智慧:十大经典策略引领稳健投资
- 把握结构性行情:精准换股策略解析
- 成交量决定股价:深度解析九句口诀的股市智慧
当前版本:V3.0

 VIP复盘网
VIP复盘网
